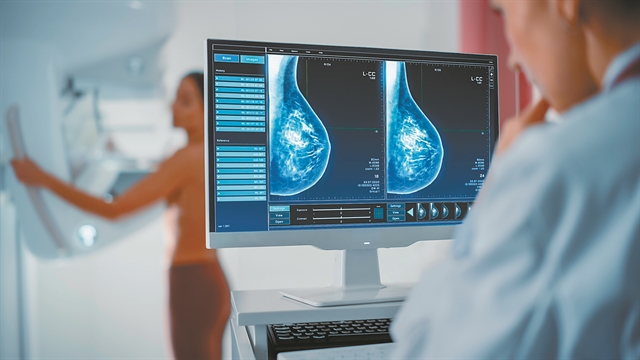
Ο καρκίνος του μαστού είναι ο πιο συχνός τύπος καρκίνου στις γυναίκες και, μόνο στην Ευρώπη, προκαλεί σχεδόν 92.000 θανάτους τον χρόνο. Παρότι ο αριθμός αυτός είναι αδιαμφισβήτητα υψηλός, τα ποσοστά επιβίωσης σημειώνουν βελτίωση. Χάρη στην πρόοδο που έχει συντελεστεί στην πρόληψη, την ανίχνευση και την αντιμετώπιση, οι ασθενείς πλέον έχουν 90% πιθανότητες επιβίωσης.
Αλλά ένας ιδιαίτερα επιθετικός υπότυπος ανατρέπει αυτή την τάση: ο τριπλά αρνητικός καρκίνος του μαστού (TNBC), που ονομάστηκε έτσι επειδή στερείται τριών ειδών κυτταρικών πρωτεϊνών. Οι καρκίνοι αυτής της κατηγορίας αποτελούν περίπου το 15% των περιπτώσεων καρκίνου του μαστού και η προοπτική είναι πολύ χειρότερη από ό,τι στους άλλους τύπους καρκίνου.
Τριπλή πρόκληση. Οι όγκοι αναπτύσσονται ταχύτερα, εξαπλώνονται συχνότερα πριν ανιχνευτούν και είναι πιθανότερο να επανεμφανιστούν ύστερα από θεραπεία. Οταν, μάλιστα, ο τριπλά αρνητικός καρκίνος του μαστού επεκταθεί σε άλλα όργανα, υπάρχει πιθανότητα πρώιμου θανάτου, ενώ τα ποσοστά επιβίωσης φτάνουν μόλις στο 11%.
Στην παρούσα φάση, δεν υπάρχει θεραπεία ειδικά για τον τριπλά αρνητικό καρκίνο του μαστού. Συνήθως αντιμετωπίζεται με χειρουργική αφαίρεση του όγκου, ακολουθούμενη από ένα «κοκτέιλ» χημειοθεραπευτικών φαρμάκων, τα οποία γνωρίζουμε ότι καταπολεμούν άλλους τύπους καρκίνου. Πολλές φορές, ωστόσο, τα αποτελέσματα είναι περιορισμένα και προσωρινά.
«Υστερα από λίγο καιρό, ο οργανισμός αναπτύσσει συχνά άμυνες ενάντια σε αυτό το κοκτέιλ και δεν είναι πια αποτελεσματικό» εξηγεί η δρ Andreia Valente, συντονίστρια ενός έργου για την εύρεση θεραπειών για τον τριπλά αρνητικό καρκίνο του μαστού, το οποίο χρηματοδοτείται από την ΕΕ. «Σε αυτή την περίπτωση μιλάμε συνήθως για πολυανθεκτικό καρκίνο, το οποίο σημαίνει ότι δεν ανταποκρίνεται πλέον σε κανέναν άλλο τύπο χημειοθεραπείας και στη συνέχεια γίνεται ιδιαίτερα επιθετικός».
Η δρ Valente, η οποία εργάζεται στο Πανεπιστήμιο της Λισαβόνας στην Πορτογαλία, και η ερευνητική συνεργάτριά της, δρ Helena Garcia, συντονίζουν την CanceRusolution, μια μονοετή πρωτοβουλία στο πλαίσιο του προγράμματος Women TechEU, που θα βρίσκεται σε εξέλιξη έως τα τέλη Μαΐου 2023.
Ενα σπάνιο μέταλλο. Οι προσπάθειες επικεντρώνονται στο ρουθήνιο, ένα σπάνιο ασημόλευκο μέταλλο, για το οποίο γνωρίζουμε ότι είναι καλά ανεκτό από τον ανθρώπινο οργανισμό. Από τα πρώτα πειράματα προκύπτει ότι το φάρμακο με βάση το ρουθήνιο που έχει αναπτύξει η ομάδα έργου αναστέλλει την ανάπτυξη των κυττάρων του τριπλά αρνητικού καρκίνου του μαστού και ταυτόχρονα εμποδίζει την εξάπλωσή τους.
Σύντομα αναμένεται να ξεκινήσει δεύτερος γύρος κλινικών μελετών, αυτή τη φορά σε ζώα. Παράλληλα, οι ερευνητές θα εξετάσουν το προφίλ ασφάλειας του φαρμάκου, προκειμένου να διασφαλίσουν ότι είναι τοξικό για τα καρκινικά κύτταρα αλλά ακίνδυνο για τον υπόλοιπο οργανισμό.
Ολοι γνωρίζουν τις βάρβαρες παρενέργειες της χημειοθεραπείας, οι οποίες μπορεί να ποικίλλουν από ναυτία και απώλεια όρεξης έως εξάντληση και τριχόπτωση, επειδή τα φάρμακα που επιτίθενται στα ταχέως αναπτυσσόμενα καρκινικά κύτταρα συνήθως σκοτώνουν και τα υγιή κύτταρα.
Τα πρώτα αποτελέσματα του έργου CanceRusolution δείχνουν ότι ένα φάρμακο με βάση το ρουθήνιο θα προκαλούσε λιγότερες παρενέργειες στις ασθενείς, επειδή φαίνεται να αφήνει άθικτα τα υγιή κύτταρα.
«Μέχρι στιγμής, από άποψη τοξικότητας, το προφίλ του φαρμάκου φαίνεται καλό» αναφέρει η δρ Garcia. «Οι μελέτες μας δείχνουν ότι ένα 24ωρο μετά τη χορήγηση του φαρμάκου η συγκέντρωσή του στον όγκο είναι υψηλή, αλλά από το περιφερικό αίμα και τα ούρα έχει σχεδόν εκκαθαριστεί. Αυτό σημαίνει ότι οι δευτερεύουσες παρενέργειες του φαρμάκου μας αναμένεται να είναι ήπιες».
Γνωρίσματα των κυττάρων. Ενα υγιές μαστικό κύτταρο είναι γεμάτο υποδοχείς – πρωτεΐνες που εκφράζονται στην επιφάνεια του κυττάρου. Αυτοί οι υποδοχείς τού επιτρέπουν να ανταποκρίνεται στις ορμόνες (για παράδειγμα, με τη διόγκωση κατά τη διάρκεια της εγκυμοσύνης) και άλλα ζωτικής σημασίας μόρια που εμπλέκονται στον έλεγχο του τρόπου με τον οποίο το κύτταρο αναπτύσσεται, διαιρείται και επιδιορθώνεται.
Υποδοχείς διαθέτουν επίσης και τα περισσότερα καρκινικά κύτταρα. Για να είναι ακριβής η διάγνωση, οι κλινικοί γιατροί αναλύουν ένα δείγμα νοσούντος μαστικού ιστού, για να διαπιστώσουν ποιοι υποδοχείς – γνωστοί εδώ ως βιοδείκτες – εκφράζονται.
Συνήθως σε όγκους του μαστού εντοπίζονται τρεις βιοδείκτες και τα φάρμακα έχουν αναπτυχθεί για να καταπολεμούν και τους τρεις.
Ο τριπλά αρνητικός καρκίνος του μαστού αποτελεί όμως εξαίρεση. Δεν διαθέτει κανέναν από αυτούς τους βιοδείκτες και, κατά συνέπεια, δεν παρέχει καμία προφανή οδό για την καταπολέμηση της ανάπτυξης του όγκου.
Επιχείρηση «δούρειος ίππος». Το φάρμακο που ανέπτυξε η ομάδα στην Πορτογαλία αντιμετωπίζει αυτό το πρόβλημα με χορήγηση του φαρμάκου ως νανοσωματιδίου που εισέρχεται στον όγκο μέσω ατελειών του συστήματος τροφοδοσίας του όγκου με αίμα. Μόλις το νανοσωματίδιο εισέλθει στον όγκο, «ανοίγει» σαν τον δούρειο ίππο, για να απελευθερώσει τη δραστική ουσία.
Στόχος αυτής της προσέγγισης είναι ένα εντελώς διαφορετικό συστατικό στοιχείο των κυττάρων του τριπλά αρνητικού καρκίνου του μαστού, ο κυτταρικός σκελετός: το πολύπλοκο δίκτυο αλληλοσυνδεόμενων πρωτεϊνικών νηματίων που συνθέτει το εσωτερικό του κυττάρου και λειτουργεί ως σκαλωσιά.
«Στη συνέχεια, το φάρμακο καταστρέφει τα θεμέλια του κυττάρου» λέει η δρ Garcia. «Χωρίς λειτουργικό κυτταρικό σκελετό, το κύτταρο δεν μπορεί σε καμία περίπτωση να επιβιώσει. Διαλύεται».
Λαμβάνοντας νέα χρηματοδότηση, οι ερευνητές πιστεύουν ότι το φάρμακο θα μπορούσε να είναι έτοιμο για αξιολόγηση στον άνθρωπο εντός δύο ετών.
Η πολυμορφία. Η αντίληψη του τριπλά αρνητικού καρκίνου του μαστού ως ενός μεμονωμένου τύπου καρκίνου του μαστού είναι υπεραπλουστευτική. Για την ακρίβεια, πρόκειται για μια εξαιρετικά ετερόκλητη κατηγορία καρκίνων.
Ωστόσο, οι ερευνητές δεν έχουν προβεί σε κατηγοριοποίηση των υπότυπων. Η κατηγοριοποίησή τους θα τους έδινε τη δυνατότητα να εντοπίσουν νέους βιοδείκτες, οι οποίοι ελπίζουμε ότι θα άνοιγαν τον δρόμο για νέες εξατομικευμένες θεραπείες.
Η κατηγοριοποίηση των ασθενών ανάλογα με τον ακριβή χαρακτήρα του όγκου τους και η επιδίωξη νέων στόχων στο πλαίσιο των θεραπειών για τον τριπλά αρνητικό καρκίνο του μαστού αποτελούν τους πυλώνες ενός ακόμα έργου που διεξάγεται με τη χρηματοδότηση της ΕΕ, του P70-IMMUNEBREAST.
Κατόπιν μελέτης 350 δειγμάτων καρκινικού ιστού, οι ερευνητές του έργου ανέπτυξαν ένα σύστημα κατηγοριοποίησης ανάλογα με την ποσότητα της «κινάσης» – ενζύμου και βιοδείκτη – που εκφράζεται από τον όγκο.
Προηγούμενη έρευνα έδειξε ότι ένα συγκεκριμένο είδος κινάσης, η P70S6K, εντοπίζεται σε υψηλά επίπεδα σε όγκους του τριπλά αρνητικού καρκίνου του μαστού.
«Αυτό το οποίο μάς ενδιαφέρει είναι η σχέση ανάμεσα σε αυτή την κινάση και την ανοσολογική απόκριση του οργανισμού» λέει η δρ Rebeca Jimeno. «Οι όγκοι αναπτύσσονται στον οργανισμό μας και – όταν όλα πάνε καλά – το ανοσοποιητικό μας σύστημα τους αναγνωρίζει και τους καταστρέφει». Το μεγάλο ερώτημα είναι γιατί αυτό το σύστημα κάποιες φορές δεν τα καταφέρνει.
Ανοσοποιητικό σύστημα. Η δρ Jimeno, η οποία εργάζεται στο Εθνικό Κέντρο Ερευνας του Καρκίνου της Ισπανίας, ανακάλυψε πως όταν εκφράζονται υψηλά επίπεδα κινάσης P70S6K, ο αριθμός των Β-κυττάρων στον όγκο είναι μικρότερος.
Τα β-κύτταρα αναγνωρίζουν, διαπερνούν και τελικά καταστρέφουν τα καρκινικά κύτταρα. Με άλλα λόγια, η P70S6K επιτρέπει στον καρκίνο να κρύβεται από το ανοσοποιητικό σύστημα και να αναπτύσσεται ανενόχλητος.
Ενα από τα επόμενα ερευνητικά βήματα είναι η εύρεση κατάλληλου αναστολέα για αυτή την κινάση. «Υπάρχουν φάρμακα που βρίσκονται σε στάδιο δοκιμών, αλλά φοβάμαι ότι θα χρειαστεί να περάσουν μερικά χρόνια μέχρι να βρεθεί κάποιο που θα είναι καλά ανεκτό από τον οργανισμό» λέει η δρ Jimeno.
Ελπίζει ότι στο τέλος θα βρεθεί μια θεραπεία. «Προσπαθούμε τόσο σκληρά να δώσουμε λύση σε αυτή τη μη αντιμετωπισμένη ανάγκη, και πιστεύω ότι σιγά-σιγά η έρευνά μας θα μας οδηγήσει σε αυτήν» αναφέρει η δρ Jimeno.